文献:
Colloidally Stabilized DSPE-PEG-Glucose/Calcium Phosphate Hybrid Nanocomposites for Enhanced Photodynamic Cancer Therapy via Complementary Mitochondrial Ca2+ Overload and Autophagy Inhibition
文献链接:https://pubs.acs.org/doi/abs/10.1021/acsami.1c11583
作者:Xuan WangYunhao LiXiongwei Deng*Fan JiaXinyue CuiJianqing Lu*Zian PanYan Wu*
通过将当前的治疗范式与互补的自噬抑制相结合以提高疗效,自噬抑制的进展推动了人们对功能化纳米平台的关注。此外,Ca2+超载也是通过增强线粒体损伤来治疗肿瘤的有前景的辅助靶点。
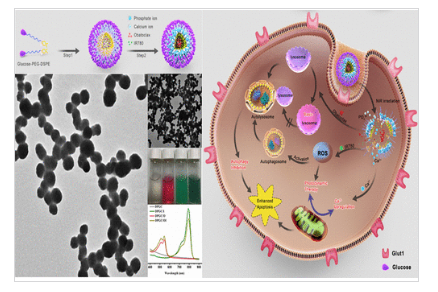
在这一观点中,互补的线粒体Ca2+超载和自噬抑制首次被证明是一种新的策略,适用于弥补光动力疗法(PDT)的不足。我们通过纳米膜生物矿化法构建了可生物降解的肿瘤靶向无机/有机杂化纳米复合材料(DPGC/OI),同步包封IR780和Obatoclax,该纳米复合材料由pH触发的磷酸钙(CP)、长循环磷脂嵌段共聚物1,2-二硬脂酰-sn-甘油-3-磷酸乙醇胺(DSPE)-聚乙二醇(PEG)2000葡萄糖(DPG)组成。
在亲水性PEG链和葡萄糖转运蛋白1(Glut-1)配体的存在下,DPGC将成为一种肿瘤导向纳米平台。随后,IR780作为一种出色的光敏剂,在激光照射后可以产生更多的有毒活性氧(ROS)。
磷酸钙(CP)作为Ca2+纳米发生器,可以在低pH值下产生Ca2+,诱导线粒体Ca2+超载。线粒体功能障碍可增加ROS的含量。基于自噬会降解功能失调的细胞器以维持代谢和稳态的前提,这可能参与对PDT的抵*,Obatoclax作为自噬抑制剂会阻碍癌症细胞的保护机制,毒性可忽略不计。DPGC/OI可以通过线粒体Ca2+超载和自噬抑制来实现这种增强的PDT。
相关推荐产品:
DSPE-PEG-CCK8
DSPE-PEG2000-GE11
DSPE-PEG2K-YIGSR
DSPE-PEG2K-RVG29
DSPE-PEG2K-MMPs
DSPE-PEG2000-NGR
DSPE-PEG-GRGDS
DSPE-PEG2K-R8
DSPE-PEG-iRGD
版权声明:
本平台根据相关科技期刊文献、教材以及网站编译整理的内容,仅用于对相关科学作品的介绍、评论以及课堂教学或科学研究。如有侵权,请联系我们删除。




 齐岳微信公众号
齐岳微信公众号 官方微信
官方微信 库存查询
库存查询