纳米复合双网络水凝胶:材料特性、制备技术与应用前景
一、材料概述
1.1 定义与核心结构
纳米复合双网络水凝胶(Nanocomposite Double Network Hydrogel, NCDNH)是一类通过将纳米材料(如纳米颗粒、纳米线、纳米片等)与双网络(Double Network, DN)凝胶体系复合,形成的兼具高力学性能、多功能响应性与结构稳定性的新型水凝胶材料。其核心结构由 “双网络基质” 与 “纳米增强相” 构成:
双网络基质:通常由第一网络(刚性、高交联密度的脆性网络,如海藻酸钠、聚丙烯酰胺)和第二网络(柔性、低交联密度的韧性网络,如聚乙烯醇、明胶)通过物理或化学作用交织形成,利用 “牺牲键断裂耗能” 机制实现基础力学强度与韧性的平衡;
纳米增强相:通过物理分散、化学接枝或原位合成等方式嵌入双网络中,既作为 “纳米交联点” 调控网络结构致密性,又通过纳米材料的高比表面积、独特物理化学性质(如导电性、光敏性、生物相容性)赋予水凝胶新增功能。
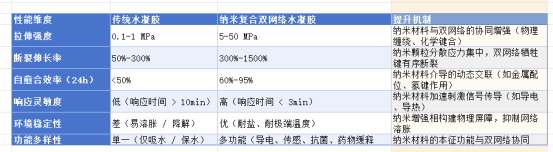
1.2 核心性能优势
相较于传统单网络水凝胶或单纯双网络水凝胶,NCDNH 的性能优势显著:
1.3 典型应用场景
NCDNH 因性能均衡性,在多个前沿领域展现应用潜力:
柔性电子与传感:作为柔性传感器的导电基底,用于人体运动监测、生理信号检测(如心率、汗液成分分析);
生物医药:作为创面修复敷料(抗菌、促愈合)、药物缓释载体(靶向递送)、组织工程支架(仿生细胞微环境);
智能材料:用于软体机器人驱动部件、形状记忆材料、环境响应型器件(如温度 / 湿度传感器);
工业与工程:作为抗冲击材料、防水密封材料、重金属离子吸附剂(废水处理)。
二、关键制备技术
NCDNH 的制备核心在于 “双网络构建” 与 “纳米材料均匀分散 / 复合”,需兼顾网络交联效率、纳米相分散性及性能协同性。以下为当前主流制备方法,含技术原理、流程及优化策略:
2.1 原位聚合法(In-situ Polymerization)
2.1.1 技术原理
先将纳米增强相均匀分散于第一网络单体溶液中,通过引发剂引发单体聚合形成第一刚性网络;随后加入第二网络单体或预聚体,通过物理交联(如冷冻 - 解冻、离子配位)或化学交联(如光固化、热聚合)形成第二柔性网络,纳米材料在聚合过程中原位嵌入双网络结构,形成稳定复合体系。
2.1.2 典型制备流程(以磷钨酸钙亚纳米线 / PVA-PAA 复合水凝胶为例)
磷钨酸水合物、四水硝酸钙、1-十八烯、油胺、PVA、丙烯酸、过硫酸铵(APS)、N,N'-亚甲基双丙烯酰胺(BIS)
原料准备
纳米增强相制备
将磷钨酸水合物与四水硝酸钙溶解于1-十八烯,加入油胺作为分散剂,60℃搅拌8h
离心(8000rpm,10min),乙醇洗涤3次,干燥获得磷钨酸钙亚纳米线
双网络原位聚合
将PVA溶解于去离子水,80℃搅拌至透明(质量分数10%),冷却至室温
加入丙烯酸单体(PVA与丙烯酸质量比1:2)、APS(引发剂,占单体总量0.5%)、BIS(交联剂,占单体总量0.1%)
加入磷钨酸钙亚纳米线(占总质量5%-10%),超声分散30min(功率200W),确保均匀分散
将混合液倒入聚四氟乙烯模具,氮气保护下60℃聚合4h,形成第一网络(PAA刚性网络)
将模具转移至-20℃冷冻24h,随后室温解冻8h,重复冷冻-解冻3次,形成第二网络(PVA物理交联柔性网络)
去离子水浸泡24h,每4h换水一次,去除未反应单体与杂质
成品:磷钨酸钙亚纳米线/PVA-PAA纳米复合双网络水凝胶
2.1.3 技术特点与优化
优势:纳米材料分散均匀,与双网络界面结合紧密,力学性能提升显著(拉伸强度可达 15-25MPa);
关键控制点:纳米材料分散(需超声 + 机械搅拌协同,避免团聚)、引发剂用量(过量易导致网络脆化)、冷冻 - 解冻次数(3 次为比较优,次数过多易导致网络断裂);
适用纳米材料:纳米线(如碳纳米管、磷钨酸钙亚纳米线)、纳米颗粒(如二氧化硅、羟基磷灰石)。
2.2 溶液共混 - 交联法(Solution Blending-Crosslinking)
2.2.1 技术原理
先分别制备双网络的两种聚合物基质溶液,再将纳米材料分散于其中一种溶液中,通过机械搅拌、超声等方式实现三者均匀混合;最后加入交联剂(物理或化学交联剂),在特定条件下(如室温、光照、离子诱导)完成双网络交联,形成纳米复合体系。该方法操作简单,适用于天然高分子与合成高分子复合体系。
2.2.2 典型制备流程(以氧化石墨烯 / 壳聚糖 - 聚丙烯酰胺复合水凝胶为例)
氧化石墨烯(GO)、壳聚糖(CS)、丙烯酰胺(AM)、APS、BIS、氯化钙(CaCl₂)
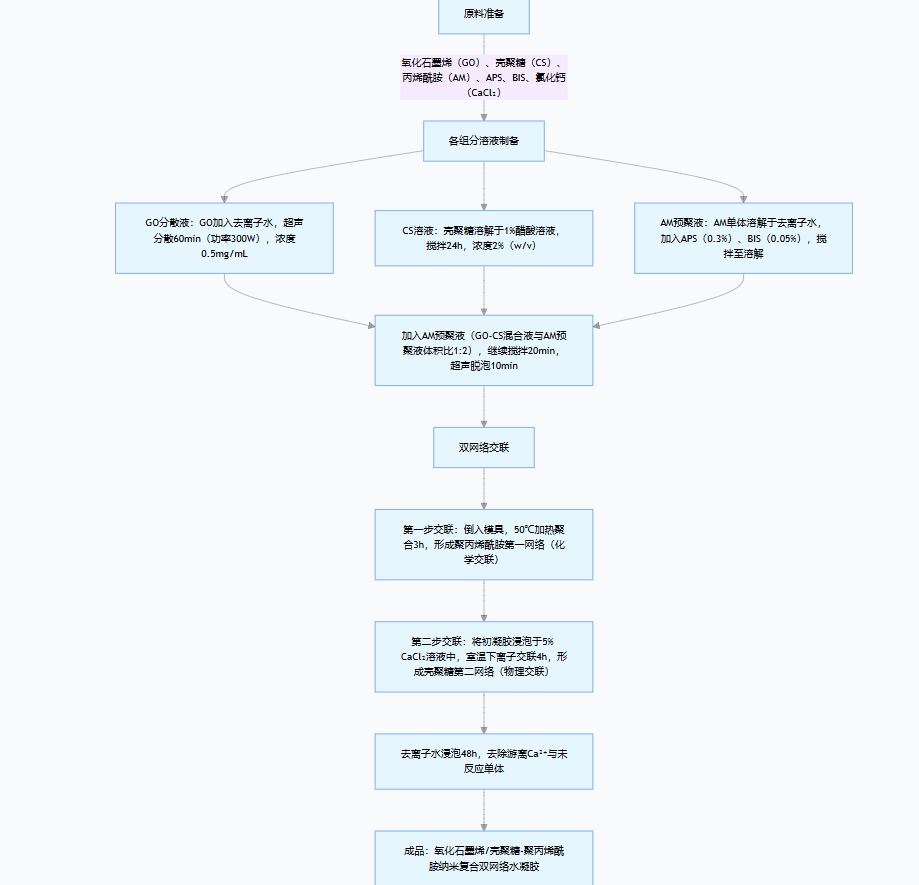
原料准备
各组分溶液制备
GO分散液:GO加入去离子水,超声分散60min(功率300W),浓度0.5mg/mL
CS溶液:壳聚糖溶解于1%醋酸溶液,搅拌24h,浓度2%(w/v)
AM预聚液:AM单体溶解于去离子水,加入APS(0.3%)、BIS(0.05%),搅拌至溶解
加入AM预聚液(GO-CS混合液与AM预聚液体积比1:2),继续搅拌20min,超声脱泡10min
双网络交联
第一步交联:倒入模具,50℃加热聚合3h,形成聚丙烯酰胺第一网络(化学交联)
第二步交联:将初凝胶浸泡于5% CaCl₂溶液中,室温下离子交联4h,形成壳聚糖第二网络(物理交联)
去离子水浸泡48h,去除游离Ca²⁺与未反应单体
成品:氧化石墨烯/壳聚糖-聚丙烯酰胺纳米复合双网络水凝胶
2.2.3 技术特点与优化
优势:操作简便、成本低,适用于大规模制备;可灵活调整双网络比例与纳米材料含量;
关键控制点:纳米材料分散性(GO 易团聚,需高功率超声 + 表面改性)、交联顺序(先化学交联刚性网络,再物理交联柔性网络,避免网络互穿不足)、Ca²⁺浓度(过高导致网络过密,韧性下降);
适用纳米材料:氧化石墨烯、MXene、纳米纤维素、金属有机框架(MOF)。
2.3 光固化 3D 打印法(Photocuring 3D Printing)
2.3.1 技术原理
将纳米材料、双网络单体(含光响应交联剂)、光引发剂混合制备光固化墨水,通过 3D 打印设备(如数字光处理(DLP)、立体光刻(SLA))控制光源(紫外光或可见光)照射,使墨水在指定区域快速聚合交联,形成第一网络;随后通过二次交联(如离子诱导、热交联)构建第二网络,最终获得定制化形状的纳米复合双网络水凝胶。该方法可精准调控水凝胶的微观结构与宏观形状,适用于高端器件制备。
2.3.2 典型制备流程(以碳纳米管 / PEGDA - 明胶甲基丙烯酰复合水凝胶为例)
多壁碳纳米管(MWCNTs)、聚乙二醇二丙烯酸酯(PEGDA)、明胶甲基丙烯酰(GelMA)、光引发剂(LAP)、去离子水
原料准备
光固化墨水制备
MWCNTs表面改性:加入KH570硅烷偶联剂,超声分散30min,增强与聚合物的相容性
将改性MWCNTs(质量分数2%-5%)加入去离子水,超声分散40min,形成稳定分散液
加入PEGDA(质量分数15%)、GelMA(质量分数10%)、LAP(质量分数0.5%),机械搅拌60min(转速800rpm),超声脱泡15min
3D打印成型第一网络
将墨水注入DLP 3D打印机料槽,设定打印参数(层厚50μm,曝光时间10s,波长405nm)
根据预设模型,光源选择性照射,使PEGDA快速光聚合,形成刚性第一网络(交联密度高)
二次交联构建第二网络
将打印成型的水凝胶浸泡于PBS缓冲液(pH7.4)中,37℃孵育24h,GelMA通过物理缠绕与氢键形成柔性第二网络
去离子水洗涤3次,去除残留光引发剂与未反应单体
成品:3D打印定制化碳纳米管/PEGDA-GelMA纳米复合双网络水凝胶
2.3.3 技术特点与优化
优势:可制备复杂形状与微观结构(如多孔结构、梯度结构);成型精度高(可达微米级);适合个性化器件与高端医疗产品(如组织工程支架);
关键控制点:墨水黏度(需控制在 1000-5000 mPa・s,确保打印流畅性)、光引发剂浓度(过低导致聚合不完全,过高影响生物相容性)、二次交联温度(37℃适配 GelMA 的物理交联,避免温度过高导致网络收缩);
适用纳米材料:碳纳米管、量子点、纳米银、羟基磷灰石(HAp)。
2.4 原位矿化 - 双网络协同法(In-situ Mineralization-Double Network Synergy)
2.4.1 技术原理
模拟生物矿化过程,在双网络水凝胶制备过程中引入矿化前驱体(如钙盐、磷酸盐),通过调控 pH、温度等条件,使无机矿物质(如羟基磷灰石、碳酸钙)在双网络中原位生长,形成 “有机双网络 - 无机纳米矿化物” 复合体系。矿化物作为纳米增强相,同时参与网络交联,显著提升水凝胶的力学性能与生物相容性,适用于生物医药领域。
2.4.2 技术特点与优化
优势:矿化物与双网络界面结合紧密(原位生长避免团聚);生物相容性优异(HAp 为人体骨骼主要成分);力学性能与生物活性协同提升;
关键控制点:矿化前驱体浓度比(Ca²⁺:PO₄³⁻=1.67:1,接近人体骨骼矿化比例)、pH 值(9.0 为 HAp 生成zui优条件)、反应温度(60℃促进矿化效率,避免明胶变性);
适用纳米材料:羟基磷灰石、碳酸钙、磷酸三钙(TCP)等生物矿化物。
三、纳米增强相的选择与作用机制
3.1 常用纳米增强相类型及特性

3.2 纳米增强相的作用机制
3.2.1 力学增强机制
物理缠绕与交联:纳米材料的高比表面积使其与双网络聚合物链形成紧密物理缠绕,同时作为 “纳米交联点” 减少网络缺陷,分散应力集中;
牺牲键作用:纳米材料与聚合物链之间的动态相互作用(如氢键、金属配位、疏水作用)在受力时可断裂耗能,避免网络整体断裂,提升韧性;
结构填充效应:纳米颗粒或纳米线填充双网络的孔隙,形成致密结构,减少形变时的网络滑移,提升拉伸强度与压缩模量。
3.2.2 功能赋予机制
本征功能延伸:纳米材料的固有性能(如碳纳米管的导电性、纳米银的抗菌性、量子点的荧光性)直接赋予水凝胶新增功能;
界面协同效应:纳米材料与双网络的界面相互作用(如 GO 与聚合物的氢键作用、MOF 与药物分子的吸附作用)增强功能协同性(如药物缓释效率、传感灵敏度);
网络调控效应:纳米材料可调控双网络的交联密度与孔隙结构(如纳米纤维素增加网络孔隙率),优化水凝胶的溶胀性能、透气性能与物质传输效率。
四、齐岳生物定制化服务与技术优势
4.1 定制化制备能力
齐岳生物针对纳米复合双网络水凝胶的科研与产业化需求,提供全方位定制化服务,涵盖:
材料体系定制:根据应用场景(如柔性电子、创面修复、组织工程)选择适配的双网络聚合物(合成 / 天然高分子)与纳米增强相(碳基、无机、MOF 等),优化材料比例与性能匹配度;
性能精准调控:通过调整纳米材料含量(0.5%-10%)、交联方式(物理 / 化学 / 光固化)、制备工艺参数,实现拉伸强度(5-50MPa)、断裂伸长率(300%-1500%)、响应时间(<3min)等关键性能的精准调控;
功能化改性:提供抗菌改性(纳米银、季铵盐接枝)、导电改性(碳纳米管、MXene 复合)、生物活性改性(HAp、生长因子负载)等功能定制,满足特定场景需求;
形状与结构定制:通过光固化 3D 打印技术,制备复杂形状、多孔结构或梯度结构的水凝胶产品,适配高端器件与医疗植入物需求。
4.2 核心技术优势
纳米分散技术:采用超声 - 机械搅拌协同 + 表面改性技术,解决纳米材料团聚问题,确保纳米增强相在双网络中均匀分散(分散粒径 < 100nm);
双网络协同交联技术:开发 “分步交联 - 原位复合” 工艺,实现刚性网络与柔性网络的高效互穿,提升力学性能与结构稳定性;
绿色制备工艺:优化原位矿化、冷冻 - 解冻等物理交联技术,减少化学交联剂用量,提升生物相容性,符合生物医药领域环保要求;
表征与检测支持:提供全面的性能表征服务,包括力学性能测试(拉伸 / 压缩试验机)、微观结构分析(SEM/TEM)、功能性能测试(导电性、抗菌性、药物缓释曲线),为科研数据提供可靠支撑。
4.3 典型应用案例
柔性传感水凝胶:定制碳纳米管 / PEGDA-PVA 纳米复合双网络水凝胶,拉伸强度达 25MPa,断裂伸长率 1200%,导电性 0.1S/m,成功应用于人体运动监测传感器;
创面修复敷料:开发纳米银 / 海藻酸钠 - 明胶复合水凝胶,抗菌率 > 99%,拉伸强度 15MPa,具备自愈合能力(24h 愈合效率 85%),加速慢性创面愈合;
组织工程支架:通过 3D 打印制备 HAp/GelMA-PEGDA 复合水凝胶支架,孔隙率 80%,力学性能匹配人体软骨组织,支持细胞黏附与增殖。
五、总结与展望
纳米复合双网络水凝胶通过 “双网络力学协同” 与 “纳米功能增强” 的创新结合,突破了传统水凝胶力学性能薄弱、功能单一的瓶颈,成为材料科学与生物医学领域的研究热点。其制备技术已从传统的溶液共混向原位聚合、3D 打印、原位矿化等精准化、功能化方向发展,未来发展趋势将聚焦于:
多功能协同集成:开发兼具力学增强、多重响应(温度 /pH/ 光)、生物活性的复合体系,适配复杂应用场景;
绿色与规模化制备:优化无溶剂、低能耗工艺,实现产业化生产;
生物医学领域深度应用:推动水凝胶在再生医学、精准医疗中的临床转化,如定制化组织工程支架、智能药物递送系统;
新型纳米增强相开发:探索二维纳米材料(如 MXene、黑磷)、智能纳米材料(如 stimuli 响应型 MOF)在双网络中的应用,拓展功能边界。
齐岳生物将持续深耕纳米复合双网络水凝胶的制备技术与应用开发,凭借定制化服务能力与核心技术优势,为科研机构与企业提供从材料设计、制备到表征的一体化解决方案,助力前沿领域的技术突破与产业升级。




 齐岳微信公众号
齐岳微信公众号 官方微信
官方微信 库存查询
库存查询