一、LNP核心定义与核心定位
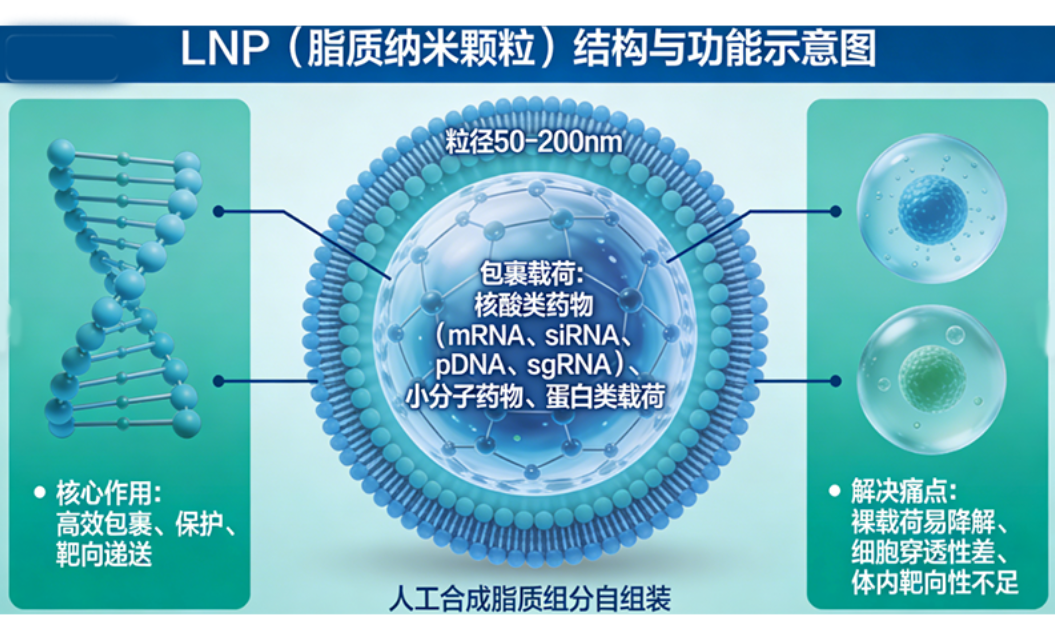
LNP,全称脂质纳米颗粒(Lipid Nanoparticle),是一种由多种人工合成脂质组分自组装形成的纳米级球形递送载体,粒径通常控制在50-200nm,模拟生物膜结构,核心作用是高效包裹、保护并靶向递送核酸类药物(mRNA、siRNA、pDNA、sgRNA等)、小分子药物及蛋白类载荷,解决裸载荷易降解、细胞穿透性差、体内靶向性不足的核心痛点。
作为当前*成熟、应用*广泛的核酸递送系统,LNP凭借高包封率、低免疫原性、可工业化放大等优势,成为mRNA疫苗、基因编辑疗法、小核酸药物的核心支撑技术,从新冠mRNA疫苗到罕见病siRNA药物,均依托LNP技术实现临床转化,是生物医药领域不可或缺的关键载体。
文献引用:Lipid nanoparticles (LNPs) are the most clinically advanced non-viral delivery systems for nucleic acid therapeutics, enabling the successful translation of mRNA vaccines and siRNA drugs from laboratory to clinic.(Zhang et al., 2023, Advanced Drug Delivery Reviews) 核心摘抄:LNP是目前临床转化*成熟的非病毒核酸递送系统,成功推动mRNA疫苗与siRNA药物从实验室走向临床应用。 |
二、LNP四大核心组分与各司其职
成熟的LNP体系由四类脂质按固定摩尔比精准配比组成,缺一不可,各组分协同完成载荷包裹、体内稳定、细胞摄取与内涵体逃逸全流程:
1. 可电离脂质(核心组分,占比40%-60%):LNP的“功能核心”,酸性条件下质子化带正电,通过静电作用紧密结合带负电的核酸载荷;生理pH下呈电中性,降低体内毒性与非特异性吸附,同时负责触发内涵体逃逸,是决定递送效率的关键。
2. 辅助磷脂(占比10%-20%):构建脂质双层结构,提升LNP结构稳定性,增强细胞膜融合能力,促进细胞摄取,常用DSPC(二硬脂酰磷脂酰胆碱)。
3. 胆固醇(占比25%-40%):填充脂质间隙,增强纳米颗粒致密性与稳定性,防止聚集,同时协助内涵体膜融合,提升载荷释放效率。
4. PEG化脂质(占比1%-3%):形成亲水保护层,延长体内循环时间,避免被免疫系统快速清除,控制颗粒粒径,防止团聚,过量会降低细胞摄取效率,需严格控制比例。
文献引用:The four-component lipid formulation (ionizable lipid, phospholipid, cholesterol, PEG-lipid) is essential for LNP stability, high nucleic acid encapsulation efficiency, and potent intracellular delivery.(Hou et al., 2021, Nature Materials) 核心摘抄:四组分脂质配方是保障LNP稳定性、高核酸包封率与高效胞内递送的核心基础。 |
三、LNP递送原理解析
LNP递送并非简单扩散,而是一套程序化的体内外协同过程,每一步均有明确的作用机制,确保载荷精准到达靶点并发挥作用:
第一步:载荷高效包裹与自组装
在酸性缓冲液体系中,可电离脂质质子化带正电,与带负电的核酸(mRNA/siRNA)通过静电相互作用结合,四类脂质同步自组装形成球形纳米颗粒,将载荷完全包裹在内部疏水核心,隔绝核酸酶与外界环境,避免载荷降解,包封率通常可达90%以上。
第二步:体内循环与靶向富集
PEG化脂质形成亲水外壳,延长体内循环半衰期,避免被单核巨噬细胞系统快速清除;未修饰LNP可通过吸附血清载脂蛋白E(ApoE),靶向结合肝细胞表面LDL受体,实现肝靶向富集;修饰靶向配体(GalNAc、*体、多肽)后,可实现肺、脾、肿瘤等组织的特异性靶向。
第三步:细胞内吞摄取
LNP通过受体介导的内吞作用进入靶细胞,被细胞膜包裹形成内涵体囊泡,此时载荷仍被包裹在LNP内部,处于内涵体隔离环境中,尚未发挥作用。
第四步:内涵体逃逸
内涵体内部pH逐渐降低(酸化至5.0-6.0),触发可电离脂质再次质子化带正电,与内涵体膜带负电的磷脂相互作用,破坏内涵体膜完整性,形成膜孔道,LNP解体,将内部载荷释放至细胞质中,避免载荷被溶酶体降解。
第五步:载荷发挥生物学功能
释放至细胞质的mRNA直接结合核糖体,翻译形成目标蛋白;siRNA启动RNA干扰通路,沉默靶基因;sgRNA/Cas9 mRNA复合物完成基因编辑,*终实现*、免疫、示踪等预期效果。
文献引用:Endosomal escape is the rate-limiting step of LNP-mediated nucleic acid delivery; ionizable lipids play a decisive role in disrupting endosomal membranes and releasing cargo into the cytoplasm.(Li et al., 2022, Nano Letters) 核心摘抄:内涵体逃逸是LNP介导核酸递送的限速步骤,可电离脂质在破坏内涵体膜、释放载荷至细胞质过程中起决定性作用。 |
四、典型案例与产品清单
(一)经典案例
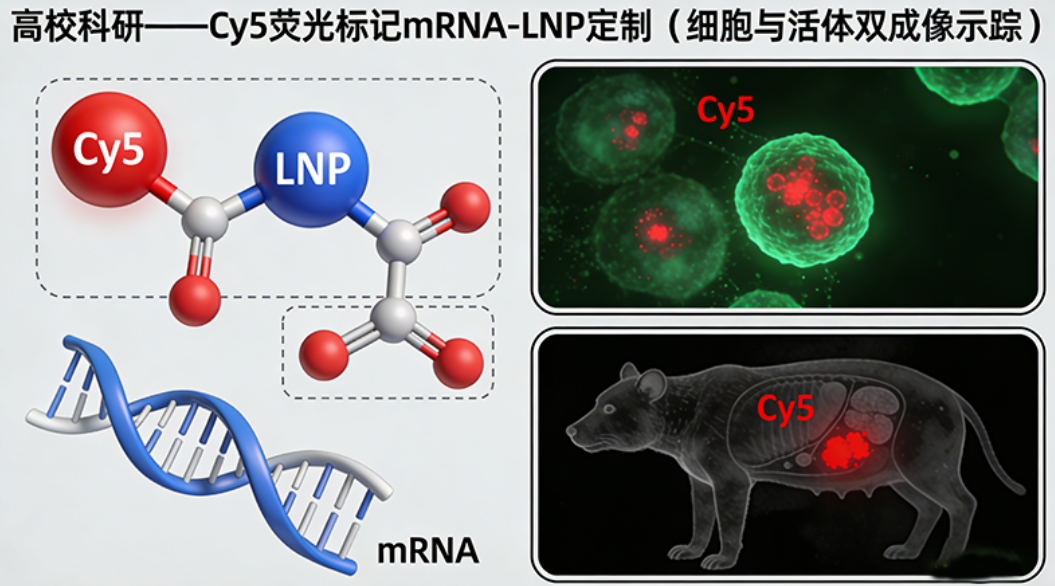
案例:高校科研——Cy5荧光标记mRNA-LNP定制(细胞与活体双成像示踪)
定制客户:某985高校生命科学学院肿瘤研究课题组
核心需求:针对肿瘤细胞mRNA递送机制研究,定制Cy5荧光标记mRNA-LNP,要求粒径80-100nm、包封率≥90%、荧光稳定性强,可同时用于体外细胞共聚焦成像与小鼠体内活体荧光示踪,无明显细胞毒性,不影响mRNA翻译表达。
(二)LNP产品列表
产品名称 | 核心组分 | 适用载荷 | 应用场景 |
通用型mRNA-LNP | DLin-MC3-DMA、DSPC、胆固醇、PEG-DMG | mRNA、circRNA | 细胞转染、动物免疫、体外蛋白表达 |
肝靶向siRNA-LNP | ALC-0315、DSPC、胆固醇、PEG-DMG | siRNA、sgRNA | 肝脏基因沉默、体内基因编辑 |
荧光标记LNP | Cy5/Cy7标记脂质、通用四组分 | 示踪探针、核酸共载 | 活体成像、细胞摄取示踪 |
高稳定性LNP | SM-102、DSPC、胆固醇、PEG-DSPE | mRNA、小分子药物 | 长效递送、低温储存 |
五、LNP产品订购流程
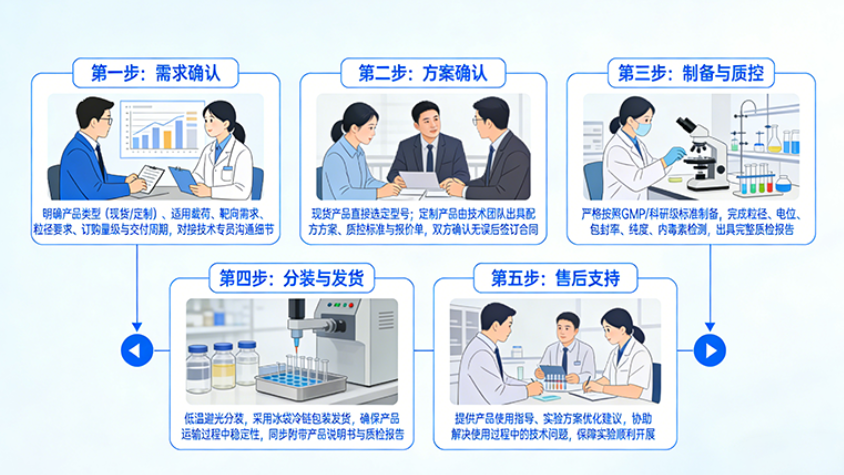
1. 需求确认:明确产品类型(现货/定制)、适用载荷、靶向需求、粒径要求、订购量级与交付周期,对接技术专员沟通细节。
2. 方案确认:现货产品直接选定型号;定制产品由技术团队出具配方方案、质控标准与报价单,双方确认无误后签订合同。
3. 制备与质控:严格按照GMP/科研级标准制备,完成粒径、电位、包封率、纯度、内毒素检测,出具完整质检报告。
4. 分装与发货:低温避光分装,采用冰袋冷链包装发货,确保产品运输过程中稳定性,同步附带产品说明书与质检报告。
5. 售后支持:提供产品使用指导、实验方案优化建议,协助解决使用过程中的技术问题,保障实验顺利开展。
六、LNP核心优势与应用场景
• 核心优势:高载荷包封率、体内稳定性强、细胞递送效率高、免疫原性低、可定制化修饰、易于工业化放大,兼容各类核酸与小分子载荷。
• 核心应用:mRNA疫苗(传染病、肿瘤)、siRNA基因沉默疗法、CRISPR/Cas9基因编辑、蛋白替代*、活体荧光示踪、靶向递药系统研发。
文献引用:LNPs have revolutionized nucleic acid therapeutics, with applications spanning infectious disease vaccines, cancer immunotherapy, and rare disease treatment, demonstrating unparalleled versatility in drug delivery.(Wang et al., 2024, Nature Reviews Drug Discovery) 核心摘抄:LNP技术革新了核酸*领域,应用覆盖传染病疫苗、肿瘤免疫、罕见病*,在药物递送中展现出无与伦比的通用性。 |




 齐岳微信公众号
齐岳微信公众号 官方微信
官方微信 库存查询
库存查询