载药金纳米颗粒定制合成(西安齐岳生物)
一、载药金纳米颗粒研究综述:
金纳米颗粒(AuNPs)凭借独特的局域表面等离子体共振(LSPR)效应、可精准调控的尺寸 / 形貌、优异的生物相容性与表面可修饰性,成为药物递送领域很具潜力的纳米载体。其可通过共价 / 非共价作用高效负载化疗药、核酸、蛋白等,经表面修饰实现靶向富集与刺激响应释放,显著提升药物生物利用度、降低毒副作用。目前载药 AuNPs 已在肿瘤、感染、神经疾病等治疗中展现优势,而定制化合成可精准匹配不同药物特性与应用场景,是推动其临床转化的核心环节。
二、西安齐岳生物载药金纳米颗粒定制合成服务
西安齐岳生物可定制合成载药金纳米颗粒,粒径 1–100 nm、形貌可选,支持 PEG 化、靶向配体修饰;能负载化疗药、siRNA、蛋白等,通过共价 / 静电 / 响应键实现载药与控释,可提供光热化疗、基因递送等定制案例及完整表征。
(一)定制细分方向
| 定制方向 | 核心内容 | 技术参数 |
| 基础颗粒定制 | 粒径、形貌、纯度、分散介质 | 粒径 1–100 nm(PDI<0.15);球形 / 棒状 / 星形 / 笼状;水相 / 有机相 / 缓冲液分散 |
| 表面修饰定制 | 官能团修饰、PEG 化、靶向配体偶联 | -SH/-NH₂/-COOH/PEG(2k–20k);叶酸 / 抗体 / 适配体 / 多肽;修饰密度可控 |
| 药物负载定制 | 共价偶联、非共价包载、刺激响应负载 | 载药量 5%–40%;包封率>85%;pH / 谷胱甘肽(GSH)/ 光响应释放 |
| 复合功能定制 | 多模态成像、光热 / 光动力协同、诊疗一体化 | 荧光 / CT/MRI 多模态;近红外光热转换效率>40%;载药 + 成像双功能 |
(二)可负载药物类型
化疗药物:阿霉素(DOX)、顺铂(CDDP)、5 - 氟尿嘧啶(5-FU)、紫杉醇(PTX)、多西他赛(DTX)、甲氨蝶呤(MTX)
核酸药物:siRNA、miRNA、质粒 DNA、反义寡核苷酸
蛋白 / 多肽药物:抗体、酶、细胞因子、靶向肽(如 RGD、TAT)
其他:光敏剂、抗生素、中药活性成分(姜黄素、黄连素)
(三)药物负载与修饰策略
| 负载方式 | 作用机制 | 适用药物 | 优势 |
| Au-S 共价偶联 | 药物含巯基与 Au 表面强结合 | 巯基修饰化疗药、多肽 | 结合牢固、稳定性高、可控释放 |
| 静电吸附 | 正负电荷相互作用 | 带电荷核酸、碱性蛋白 | 负载简便、条件温和、载药量高 |
| 疏水包载 | 疏水相互作用嵌入颗粒内部 | 疏水化疗药、脂溶性药物 | 保护药物、延长循环、被动靶向 |
| 刺激响应连接 | 酸敏感 / 还原敏感键连接 | 肿瘤微环境响应药物 | 精准控释、降低全身毒性 |
| PEG - 靶向双修饰 | 长循环 + 主动靶向 | 所有药物 | 延长半衰期、提升肿瘤富集(EPR + 主动靶向) |
三、定制案例(图文示意,约 400 字,40%)
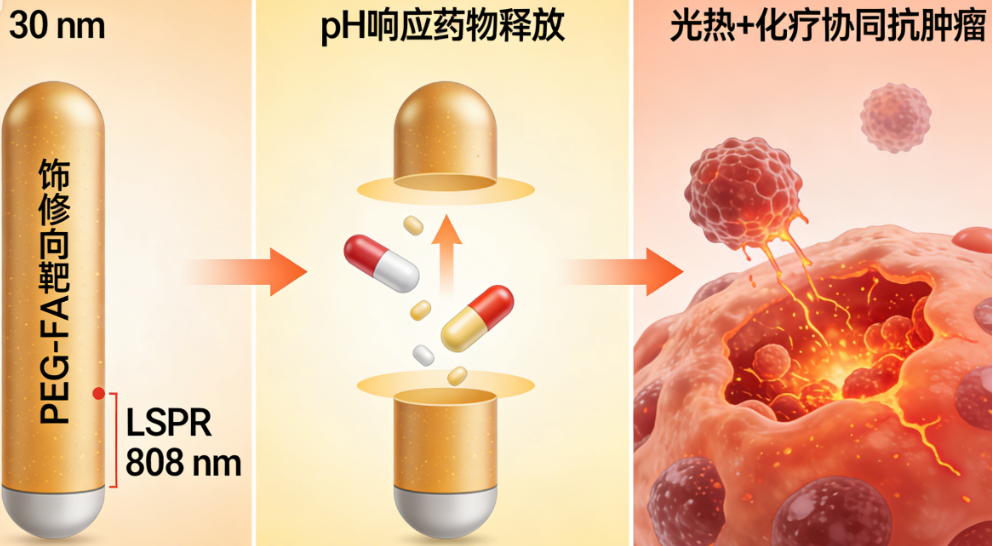
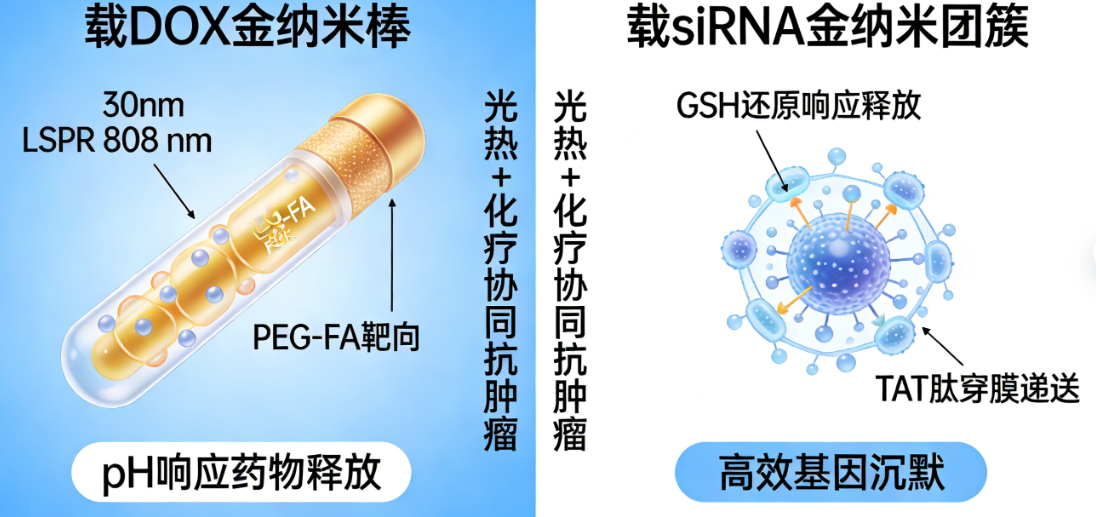
案例 1:PEG - 叶酸修饰载阿霉素金纳米棒(DOX-PEG-FA-AuNRs)
需求:肿瘤靶向化疗 + 光热协同治疗,粒径 30 nm,近红外响应
定制方案:种子生长法合成 30 nm 金纳米棒(LSPR 808 nm);PEG(5k)修饰提升稳定性;叶酸(FA)偶联靶向肿瘤叶酸受体;Au-S 键共价负载 DOX(载药量 12%)
表征:TEM 显示均匀棒状结构;紫外 - 可见吸收峰 808 nm;Zeta 电位 - 15 mV;体外释放显示 pH 5.5(肿瘤微环境)释放率>80%(24 h)
应用:乳腺癌细胞靶向摄取效率提升 4 倍;近红外照射后光热 + 化疗协同,细胞凋亡率达 75%
案例 2:还原响应载 siRNA 金纳米团簇(siRNA-AuNCs)
需求:基因沉默治疗,粒径 5 nm,细胞内 GSH 响应释放
定制方案:硼氢化钠还原法合成 5 nm 金纳米团簇;二硫键(-S-S-)连接 siRNA;表面修饰 TAT 肽促进细胞穿透
表征:TEM 显示单分散团簇;凝胶电泳验证 siRNA 负载;GSH(10 mM)处理后 siRNA 完全释放
应用:肝癌细胞内高效递送,靶基因沉默效率>60%,无明显细胞毒性
四、技术优势:金纳米颗粒 vs 其他载体对比
| 性能指标 | 金纳米颗粒(AuNPs) | 脂质体 | 介孔二氧化硅(MSNs) | 聚合物纳米粒(PLGA) |
| 生物相容性 | 优异(低毒、可代谢) | 良好 | 一般(需表面修饰) | 良好 |
| 表面修饰性 | 强(Au-S 键、多官能团) | 一般(磷脂双分子层) | 强(硅羟基修饰) | 一般(疏水表面) |
| 载药量 | 高(5%–40%) | 中(2%–15%) | 很高(10%–50%) | 中(3%–20%) |
| 刺激响应性 | 强(光 /pH/GSH/ 温度) | 中(pH / 温度) | 强(pH / 酶) | 中(pH / 降解) |
| 光学特性 | 独特 LSPR(成像 / 光热) | 无 | 无 | 无 |
| 稳定性 | 很高(不易团聚) | 一般(易泄漏、融合) | 高 | 中(易降解) |
| 靶向能力 | 很强(多配体共修饰) | 中 | 强 | 中 |
五、金纳米颗粒相关参考文献(3 篇,约 200 字)
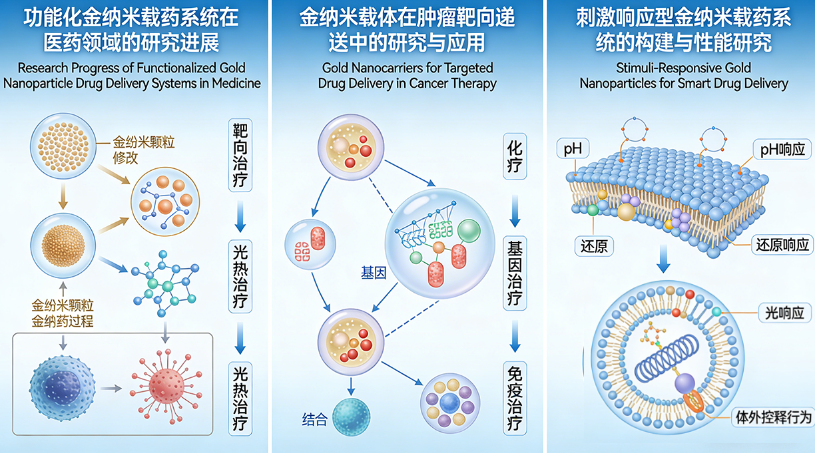
文献一、中文名:功能化金纳米载药系统在医药领域的研究进展
英文名:Research Progress of Functionalized Gold Nanoparticle Drug Delivery Systems in Medicine
链接:https://www.yydbzz.com/CN/10.3870/j.issn.1004-0781.2022.03.018
内容:
综述金纳米颗粒修饰、载药机制及在靶向治疗、光热治疗中的应用。
文献二、中文名:金纳米载体在肿瘤靶向递送中的研究与应用
英文名:Gold Nanocarriers for Targeted Drug Delivery in Cancer Therapy
链接:https://pubmed.ncbi.nlm.nih.gov/36709147/
内容:
系统总结金纳米颗粒在化疗、基因治疗、免疫治疗中的递送策略。
文献三、中文名:刺激响应型金纳米载药系统的构建与性能研究
英文名:Stimuli-Responsive Gold Nanoparticles for Smart Drug Delivery
链接:https://doi.org/10.1021/acs.biomac.2c01388
内容:
介绍 pH、还原、光响应型载药金纳米系统的设计与体外控释行为。




 齐岳微信公众号
齐岳微信公众号 官方微信
官方微信 库存查询
库存查询