西安齐岳生物科技有限公司依托有机合成、生物修饰及纳米载体三大核心技术平台,聚焦前体药物定制与药物修饰、改性领域,为科研院校、药企研发部门及创新生物技术团队,提供从分子设计、合成制备、纯化表征到技术支持的一站式定制化服务,精准解决药物研发过程中水溶性差、靶向性弱、毒性偏高、生物利用度低等核心痛点,助力药物研发效率提升与成果转化。

第一部分:定制内容
西安齐岳生物定制服务核心覆盖三大板块,各板块细分方向明确、技术成熟,可根据客户研发需求灵活调整,适配毫克级科研样品至克级中试产品的全场景,具体如下:
一、前体药物定制
核心目标:精准激活、靶向递送、降低毒性,使药物在正常生理环境中保持惰性,仅在病灶部位通过特定机制激活释放活性药物。
1. 病灶微环境响应型前体药物定制
适配病灶特异性微环境,实现精准激活释放,细分3类:
• 低pH响应型:适配肿瘤(pH 6.0-6.8)、炎症组织(pH 5.5-6.5),通过腙键、缩醛键等酸敏连接基设计,酸性环境下释药。
• 氧化还原响应型:适配肿瘤细胞内高谷胱甘肽(GSH)浓度,通过二硫键修饰,在肿瘤细胞内还原裂解释药。
• 酶响应型:适配肿瘤/炎症组织高表达的MMP、组织蛋白酶、酯酶等,通过酶特异性肽键、酯键设计,酶促裂解激活药物。
2. 靶向配体介导型前体药物定制
核心:化学偶联靶向分子与前药骨架,实现“主动靶向+环境激活”双重调控,提升病灶富集度、降低脱靶毒性。
可定制靶向配体:小分子配体(叶酸、半乳糖、生物素等)、多肽类(RGD多肽、肿瘤特异性靶向肽等)、抗体/抗体片段、核酸适配体。
3. 多功能协同型前体药物定制
核心:整合靶向激活、联合给药、可视化追踪等功能,适配耐药性、转移性肿瘤研发需求,细分3类:
• 化疗-核酸协同前药:如化疗药-siRNA偶联前药
• 化疗-光动力协同前药:如光敏剂-化疗药偶联前药
• 荧光标记可视化前药:荧光染料-前药偶联物,用于体内分布追踪
4. 载体包覆型前体药物定制
核心:生物相容性载体包裹前药,实现靶向递送与环境响应协同,提升体内循环稳定性与病灶穿透能力。
可定制载体:聚合物纳米粒(PEG-PLA、PLGA等)、金属有机框架(MOF,如ZIF-8)、脂质体、细胞膜包被纳米载体、智能微针。
二、药物结构修饰
核心目标:针对现有药物结构缺陷,通过精准化学修饰,优化理化性质与药理活性,解决稳定性差、溶解性不佳、特异性弱等问题。
1. 小分子药物修饰
适配阿霉素、紫杉醇、顺铂、青蒿琥酯等小分子化疗药、抗炎药,细分4类:
• PEG修饰:提升水溶性、延长体内循环时间
• 酰化修饰:增强药物稳定性
• 胺化修饰:改善药物靶向性
• 糖基化修饰:提升生物相容性
2. 生物大分子药物修饰
适配蛋白、多肽、核酸类药物(抗体、胰岛素、siRNA等),解决易降解、半衰期短、免疫原性高的问题。
可提供服务:PEG修饰、荧光标记修饰、糖基化修饰、小分子药物/靶向配体偶联修饰。
3. 药物活性基团修饰
对药物分子中羟基、羧基、氨基、巯基等活性基团精准修饰,调控脂水分配系数、代谢速率,增强靶点结合能力,降低代谢毒性,助力构效关系研究。
三、药物性能改性
核心目标:优化药物物理、化学及生物性能,解决研发与应用中的关键难题,适配不同治疗场景。
1. 水溶性改性
针对紫杉醇、姜黄素等难溶性药物,通过增溶修饰、载体包覆、纳米化等技术,提升水溶性,降低制剂难度,提高吸收效率。
2. 稳定性改性
通过化学修饰(交联、活性基团保护)、载体改性(MOF包覆、脂质体包裹),提升药物储存、运输及体内稳定性,减少降解,延长有效期与体内半衰期。
3. 靶向性改性
结合靶向配体偶联、载体表面修饰技术,使药物特异性识别病灶细胞,精准递送,减少正常组织损伤,提升治疗效果。
4. 缓释/控释改性
通过载体改性(缓释微球、控释凝胶)、结构修饰(长效化修饰),实现药物缓慢、匀速或响应性释放,延长作用时间,减少给药次数,提升用药安全性。
第二部分:定制案例
案例一:氧化还原响应型阿霉素前体药物定制
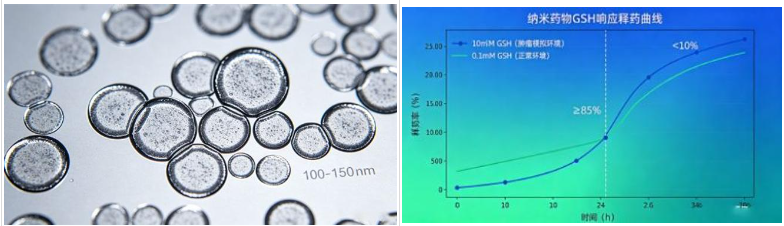
客户需求:解决阿霉素(DOX)心脏毒性强、靶向性弱、易耐药问题,定制氧化还原响应型前体药物,正常生理环境稳定,肿瘤细胞内(高GSH)快速释药。
定制方案:以二硫键为连接基,将DOX与PEG-PLA聚合物偶联,合成mPEG-PLA-SS-DOX前药,自组装形成纳米胶束;肿瘤细胞内高GSH还原二硫键释药,PEG修饰提升水溶性与循环稳定性。
案例二:pH敏感型青蒿琥酯前体药物定制
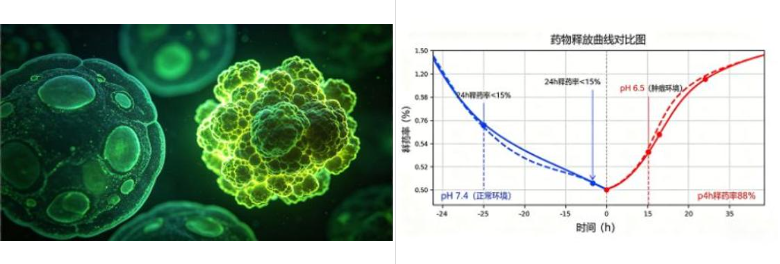
客户需求:定制pH敏感型青蒿琥酯(ART)前药,适配肿瘤酸性微环境,解决ART水溶性差、生物利用度低、正常组织毒性问题,用于耐药性肿瘤研究。
定制方案:ART与可降解聚β-氨基酯(PBAE)通过酸敏键连接,构建PBAE-ART前药纳米粒子;肿瘤酸性环境(pH 6.0-6.5)下聚合物链断裂释药,PEG修饰提升水溶性与循环稳定性。
第三部分:典型高分文献摘抄及翻译
文献一:The Delicate Disulfide-Acryloyl Modification of Prodrug Facilitates Precise Albumin Targeting, Enhanced Tumor Accumulation, and Reduced Toxicity
期刊信息:ACS Publications(IF:7.419,属于药物化学领域TOP期刊),文献链接:https://pubs.acs.org/doi/abs/10.1021/acs.jmedchem.5c01094(对应本文献引用链接1)
原文摘抄:Doxorubicin (DOX), a widely used chemotherapy, suffers from severe cardiotoxicity. Doxil, the first FDA-approved antitumor nanoformulation, mitigates the cardiotoxicity of DOX, but fails to enhance therapeutic efficacy probably due to limited cellular uptake and restricted drug release. To overcome these challenges, this study developed a novel disulfide-acryloyl-modified DOX prodrug (DSSA) for albumin-targeted drug delivery. DSSA could self-assemble into stable nanoassemblies (DSSA NPs) with a high drug-loading capacity (65.46%). DSSA NPs could covalently bind to endogenous albumin, significantly enhancing pharmacokinetics with a nearly 40-fold increase in the area under the curve (AUC) compared to DOX solution (DOX sol) and achieving over twice the tumor accumulation of DOX sol and Doxil. Additionally, the reduction-responsive disulfide bonds enabled selective drug release in tumor microenvironments, minimizing off-target toxicity. These results demonstrate the potential of disulfide-acryloyl modification as a promising prodrug strategy to enhance tumor targeting and safety in chemotherapeutic delivery. Subjects: Biopolymers.
中文翻译:阿霉素(DOX)是一种广泛使用的化疗药物,但存在严重的心脏毒性。多柔比星脂质体(Doxil)是首个获得美国食品药品监督管理局(FDA)批准的抗肿瘤纳米制剂,虽能减轻阿霉素的心脏毒性,但由于细胞摄取有限且药物释放受限,未能提升治疗效果。为克服这些挑战,本研究开发了一种新型二硫键-丙烯酰基修饰的阿霉素前体药物(DSSA),用于白蛋白靶向药物递送。DSSA可自组装形成稳定的纳米组装体(DSSA NPs),药物负载率高达65.46%。DSSA NPs能与内源性白蛋白共价结合,显著改善药代动力学特性,与阿霉素溶液(DOX sol)相比,血药浓度-时间曲线下面积(AUC)提升近40倍,肿瘤富集量是DOX sol和Doxil的2倍以上。此外,还原响应性二硫键可实现肿瘤微环境中的选择性药物释放,最大限度降低脱靶毒性。这些结果表明,二硫键-丙烯酰基修饰作为一种极具潜力的前体药物策略,可在化疗递送中提升肿瘤靶向性和安全性。研究方向:生物聚合物。
文献二:Structural Modification in Anesthetic Drug Development for Prodrugs and Soft Drugs
期刊信息:Frontiers in Pharmacology(IF:5.988,属于药理学领域核心期刊),文献链接:https://public-pages-files-2025.frontiersin.org/journals/pharmacology/articles/10.3389/fphar.2022.923353/pdf(对应本文献引用链接2)
原文摘抄:Among the advancements in drug structural modifications, the increased focus on drug metabolic and pharmacokinetic properties in the anesthetic drug design process has led to significant developments. Drug metabolism also plays a key role in optimizing the pharmacokinetics, pharmacodynamics, and safety of drug molecules. Thus, in the field of anesthesiology, the applications of pharmacokinetic strategies are discussed in the context of sedatives, analgesics, and muscle relaxants. In this review, we summarize two approaches for structural optimization to develop anesthetic drugs, by designing prodrugs and soft drugs. Drugs that both failed and succeeded during the developmental stage are highlighted to illustrate how drug metabolism and pharmacokinetic optimization strategies may help improve their physical and chemical properties.
中文翻译:在药物结构修饰的研究进展中,麻醉药物设计过程中对药物代谢和药代动力学特性的关注度不断提高,推动了该领域的重大发展。药物代谢在优化药物分子的药代动力学、药效学和安全性方面也发挥着关键作用。因此,在麻醉学领域,药代动力学策略的应用主要围绕镇静药、镇痛药和肌肉松弛药展开。本综述总结了两种用于麻醉药物研发的结构优化方法,即前体药物设计和软药设计。本文重点介绍了研发阶段中成功与失败的药物案例,以说明药物代谢和药代动力学优化策略如何帮助改善药物的物理和化学性质。
第四部分:文献引用链接
1. https://pubs.acs.org/doi/abs/10.1021/acs.jmedchem.5c01094(对应文献一,二硫键修饰前体药物研究)
2. https://public-pages-files-2025.frontiersin.org/journals/pharmacology/articles/10.3389/fphar.2022.923353/pdf(对应文献二,麻醉药物前体药物结构修饰研究)
3. https://pubs.rsc.org/en/content/articlehtml/2023/cs/d2cs00673a(小分子前药用于癌症化疗和光学治疗的设计策略综述)
4. https://pubmed.ncbi.nlm.nih.gov/41061162/(药物水溶性和通透性改善的化学修饰策略研究)
5. https://pmc.ncbi.nlm.nih.gov/articles/PMC11219257/pdf/nihms-1982118.pdf(自裂解键在药物设计中的应用研究)
6. https://pubs.acs.org/doi/10.1021/acs.biomac.3c00287(MOF载体在前体药物递送中的应用研究)
7. https://www.sciencedirect.com/science/article/pii/S0169409X2200156X(PEG修饰在生物大分子药物中的应用研究)
8. https://pubs.acs.org/doi/10.1021/acs.jmedchem.2c00876(酶响应型前体药物的设计与应用研究)
9. https://www.sciencedirect.com/science/article/pii/S000930842300087X(pH响应型脂质体前体药物的研发与评价)
10. https://pubmed.ncbi.nlm.nih.gov/35133794/(药物修饰中自组装技术的应用研究)
11. https://pubs.acs.org/doi/10.1021/acs.jpharmcas.3c00052(前体药物的体内代谢与药效评价研究)
第五部分:部分产品展示
中文名称 | 英文名称 | 产品类型 |
二硫键修饰阿霉素前体药物 | mPEG-PLA-SS-DOX Prodrug | 氧化还原响应型前体药物 |
pH敏感型青蒿琥酯前体药物 | PBAE-ART Prodrug | pH响应型前体药物 |
PEG修饰顺铂大分子药物 | PAsp-PEG-CDDP Macromolecular Drug | 药物修饰/改性产品 |
叶酸靶向MOF包覆阿霉素前体药物 | FA-DOX@ZIF-8 Prodrug | 靶向载体包覆型前体药物 |
MMP响应型紫杉醇前体药物 | MMP-Responsive Paclitaxel Prodrug | 酶响应型前体药物 |
荧光标记阿霉素前体药物 | CY3-DOX Prodrug | 多功能协同型前体药物 |
PEG修饰胰岛素 | PEG-Modified Insulin | 生物大分子药物修饰产品 |
5-氟尿嘧啶-壳聚糖-聚乙二醇单甲醚大分子前药 | 5-FU-CS-mPEG Prodrug | 大分子前体药物 |
pH敏感型阿霉素聚合物前药 | PAMAM-PEG-C12-hyd-DOX Prodrug | pH响应型前体药物 |
半乳糖靶向阿霉素前药 | Gal-DOX Prodrug | 靶向配体介导型前体药物 |
姜黄素-PEG-PLA前药胶束 | Curcumin-PEG-PLA Prodrug Micelles | 氧化还原响应型前体药物 |
脂质体包裹紫杉醇前药 | Paclitaxel-Liposome Prodrug | 载体包覆型前体药物 |
PEG修饰siRNA | PEG-Modified siRNA | 核酸类药物修饰产品 |
RGD多肽修饰紫杉醇前药 | RGD-Modified Paclitaxel Prodrug | 靶向配体介导型前体药物 |
藤黄酸-pH敏感脂质体 | Gambogenic Acid-pH Sensitive Liposome (GNA-PLS) | pH响应型载体包覆前体药物 |




 齐岳微信公众号
齐岳微信公众号 官方微信
官方微信 库存查询
库存查询