西安齐岳生物 提供PEG修饰蛋白全品类定制服务,涵盖线性、Y型、多臂PEG等多种修饰类型。支持分子量范围200 Da–40 kDa按需选择,可根据不同应用场景进行灵活设计。

一、定制内容
结合不同应用场景与蛋白特性,细分4大定制方向,可灵活组合调整,满足个性化需求:
(一)PEG类型定制
• 线性PEG修饰:结构简单、空间位阻小,适用于对蛋白活性影响要求高、需保留原有功能结构的场景(如诊断酶、小分子蛋白修饰),可实现单端或双端修饰,末端官能团可定制(羟基、氨基、羧基等)。
• Y型PEG修饰:分支结构,空间稳定性强,能显著延长蛋白体内半衰期、降低免疫原性,适用于长效蛋白药物研发(如重组凝血因子、生长激素修饰),修饰后蛋白生物活性保留率高。
• 多臂PEG修饰:多分支结构(4臂、6臂、8臂等),可实现多位点修饰,能大幅提升蛋白稳定性、改善溶解性,适用于工业酶催化、纳米递送系统等场景,可增强蛋白在*端环境(高温、强酸强碱)下的耐受性。
(二)分子量定制
分子量覆盖200Da–40kDa,按需精准选型,匹配不同应用需求:
• 低分子量(200Da–5kDa):适用于小分子蛋白、多肽修饰,减少空间位阻,避免影响蛋白活性位点,常用于科研实验、诊断试剂标记。
• 中分子量(5kDa–20kDa):平衡活性与稳定性,适用于多数工业酶、常规科研蛋白修饰,兼顾催化活性与*降解能力。
• 高分子量(20kDa–40kDa):重点提升蛋白半衰期、增强稳定性,适用于长效蛋白药物、体内成像用蛋白修饰,可显著降低体内清除速率。
(三)修饰位点定制
• 定点修饰:通过分子模拟与结构分析,精准选择蛋白表面暴露、远离活性中心的氨基酸残基(赖氨酸、半胱氨酸等)进行修饰,*大限度保留蛋白活性,适用于药物研发、高活性酶修饰。
• 随机修饰:针对无需精准位点控制的场景(如工业酶粗品修饰),实现快速修饰,提升效率、降低成本,满足规模化应用需求。
(四)功能化定制
• 荧光/靶向修饰:结合PEG修饰引入荧光基团或靶向分子,适用于蛋白定位、体内成像、靶向递送等科研与药物研发场景。
• 稳定性优化定制:针对易自溶、易聚集的蛋白(如胰蛋白酶),通过PEG修饰优化其热稳定性、pH耐受性和储存稳定性,延长保质期与使用寿命。
二、具体产品
依托全品类PEG原料与成熟修饰技术,可定制以下核心产品(可按需调整参数):
产品类型 | PEG类型 | 分子量范围 | 应用场景 |
PEG修饰胰蛋白酶 | 线性/多臂 | 5kDa–20kDa | 工业催化、蛋白水解、生物分析 |
PEG修饰荧光素酶 | Y型/多臂 | 20kDa–40kDa | 体内生物发光成像、ATP检测 |
PEG修饰重组凝血因子VIII | Y型 | 40kDa | 长效血友病*药物研发 |
PEG修饰干扰素α | 线性/Y型 | 10kDa–30kDa | *病毒药物研发、科研实验 |
PEG修饰工业酶(淀粉酶/脂肪酶) | 多臂 | 5kDa–15kDa | 食品加工、工业催化 |
GMP级PEG修饰蛋白 | 全类型 | 5kDa–40kDa | 临床前药物研发、药物申报 |
三、案例分享
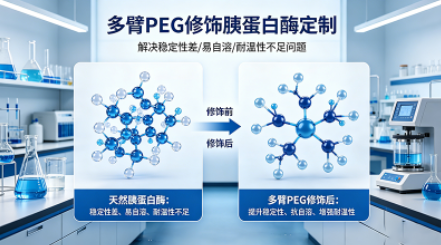
案例1:多臂PEG修饰胰蛋白酶定制
需求背景:某食品加工企业需定制PEG修饰胰蛋白酶,解决天然胰蛋白酶在工业催化过程中稳定性差、易自溶、耐温性不足的问题,提升蛋白水解效率并降低使用成本。
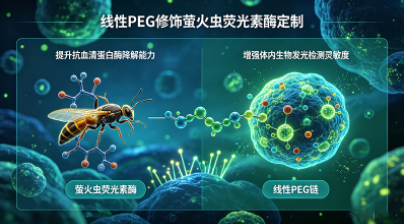
案例2:线性PEG修饰荧光素酶定制
需求背景:某科研机构开展体内生物发光成像研究,需定制PEG修饰萤火虫荧光素酶,提升其抗血清蛋白酶降解能力,增强检测灵敏度。
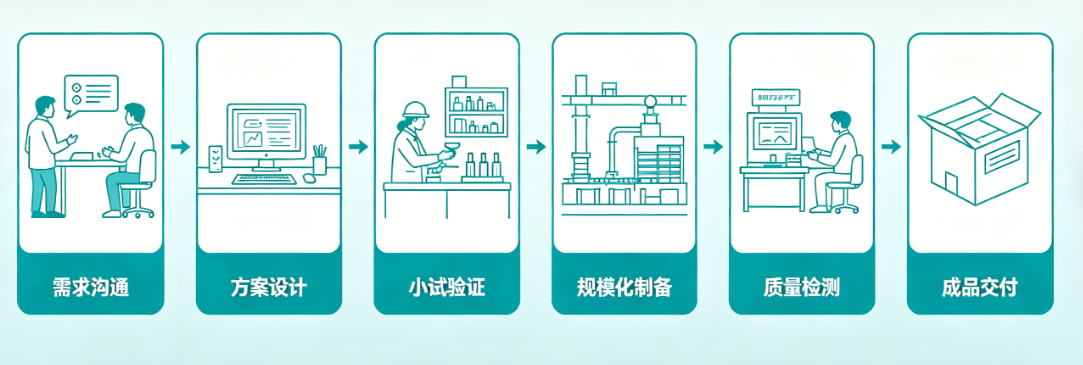
四、服务流程
1. 需求沟通:明确客户蛋白类型、PEG类型、分子量、修饰位点及应用场景,评估定制可行性;
2. 方案设计:结合蛋白结构与需求,制定个性化修饰方案,确认工艺参数与交付标准;
3. 小试验证:进行小批量修饰实验,优化反应条件,验证修饰效果与蛋白活性;
4. 规模化制备:按优化方案进行批量修饰,通过凝胶过滤、液相色谱等工艺纯化;
5. 质量检测:检测蛋白纯度、修饰度、活性等指标,出具检测报告;
6. 成品交付:按客户要求包装,同步交付技术资料与检测报告。
五、参考文献
1. Li Y, et al., “Site-specific PEGylation of trypsin: improving stability and activity,” Biotechnol Bioeng, 2019.
2. Wang X, et al., “PEGylated trypsin derivatives: synthesis and characterization,” J Mol Catal B Enzym, 2020.
3. Chen H, et al., “Site-directed PEGylation strategies for enzymes,” Protein Expr Purif, 2018.
4. Veronese F.M., Pasut G., PEGylation, successful approach to drug delivery, Drug Discovery Today, 2005.
5. Roberts M.J. et al., Chemistry for peptide and protein PEGylation, Advanced Drug Delivery Reviews, 2012.
6. Zhang X , Wang H , Ma Z , et al. Effects of pharmaceutical PEGylation on drug metabolism and its clinical concerns(J). Expert Opinion on Drug Metabolism & Toxicology, 2014, 10(12):1691-702.
7. Kozma G T , Shimizu T , Ishida T , et al. Anti-PEG antibodies: Properties, formation and role in adverse immune reactions to PEGylated nano-biopharmaceuticals(J). Advanced Drug Delivery Reviews, 2020.
8. Zhang L, et al., “Applications of PEGylated trypsin in industrial catalysis and protein analysis,” Process Biochem, 2021.




 齐岳微信公众号
齐岳微信公众号 官方微信
官方微信 库存查询
库存查询