第一部分 西安齐岳生物定制合成服务详情
西安齐岳生物深耕磷脂分子定制合成领域,聚焦疏水链修饰的磷脂分子定向设计与精准合成,依托完善的研发体系、专业的技术团队及标准化生产流程,可根据客户科研、生产及应用场景的差异化需求,提供全流程定制服务,核心围绕疏水链修饰为核心,联动磷脂分子亲水头基、连接臂及功能基团的协同调控,实现“定向设计-精准合成-纯度检测-样品交付”一站式服务,定制内容专业细分如下,覆盖多领域应用需求,确保每一项定制都贴合客户实验及生产痛点。
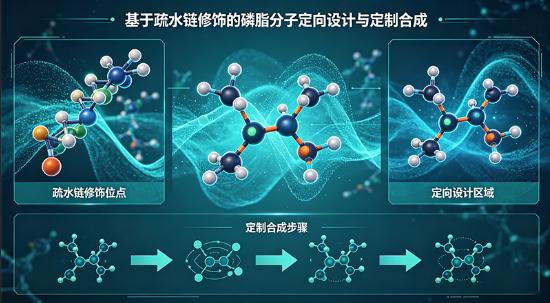
一、疏水链核心修饰定制
疏水链作为磷脂分子两亲性结构的核心疏水区,其结构参数直接决定磷脂分子的膜流动性、相变温度、堆积密度及自组装性能,西安齐岳生物可针对疏水链进行多维度精准修饰,满足不同应用场景对磷脂疏水性的差异化要求,具体定制方向如下:
• 疏水链长度定制:可定向设计并合成不同碳链长度的疏水链修饰磷脂,碳链长度覆盖C6-C22,涵盖短链(C6-C10)、中链(C11-C16)、长链(C17-C22),可根据客户需求精准调控,例如短链疏水链可提升磷脂分子的水溶性及分散性,适用于纳米载体的快速制备;长链疏水链可增强磷脂双分子层的稳定性,适用于长效药物递送体系及人工细胞膜构建,同时可提供混合碳链长度的定制的服务,实现疏水性与膜性能的精准匹配。
• 疏水链饱和度定制:针对疏水链的不饱和程度进行定向修饰,可定制全饱和、单不饱和、多不饱和疏水链修饰磷脂,例如全饱和疏水链(如硬脂酰链)可提升磷脂膜的刚性及稳定性,降低膜流动性,适用于高温环境下的应用;不饱和疏水链(如油酰链、亚油酰链)可增强膜的柔性及流动性,助力内涵体逃逸,适用于基因递送、细胞转染等场景,同时可精准控制不饱和键的数量及位置,避免氧化失效,保障产品稳定性。
• 疏水链官能团修饰定制:在疏水链末端或侧链引入特定官能团,实现磷脂分子的功能拓展,可定制的官能团包括但不限于巯基(-SH)、羧基(-COOH)、氨基(-NH2)、炔基(-C≡CH)、叠氮基(-N3)、酯基(-COOR)及醚键(-O-)等,其中醚键修饰可提升磷脂的抗酶解能力,巯基、羧基等活性官能团可用于后续生物偶联反应,适配纳米载体构建、界面修饰及生物偶联体系,满足客户对磷脂分子功能化的深层需求。
• 疏水链分支结构定制:可设计并合成具有分支结构的疏水链修饰磷脂,通过调控分支数量、分支长度,优化磷脂分子的自组装行为,改善磷脂膜的通透性、韧性及与生物分子的相互作用,适用于特殊生物传感、膜蛋白研究及新型脂质体构建等高端科研场景,填补常规直链疏水链磷脂的应用局限。
二、磷脂分子协同定制
基于疏水链修饰的核心,同步提供磷脂分子其他结构模块的协同定制,实现分子结构与应用场景的精准匹配,提升定制产品的适用性,具体包括:
• 亲水头基定制:可根据客户需求替换或修饰磷脂分子的亲水头基,涵盖磷脂酰胆碱(PC)、磷脂酰乙醇胺(PE)、磷脂酰丝氨酸(PS)、磷脂酰甘油(PG)等常规头基,同时可进行阳离子、阴离子修饰,或接枝聚乙二醇(PEG)形成亲水层,提升磷脂分子的水溶性、体内长循环能力,降低非特异性吸附,适配靶向递送、蛋白/核酸偶联等场景,例如PEG化修饰可延长磷脂纳米载体的体内循环半衰期,助力肿瘤靶向富集。
• 连接臂定制:在疏水链与亲水头基之间,或疏水链与功能基团之间,定制不同长度、不同类型的连接臂(如PEG连接臂、烷基连接臂、肽段连接臂),调控功能基团的空间位阻,优化磷脂分子的自组装性能及生物相容性,同时可引入pH敏感腙键、还原敏感二硫键等响应型连接臂,实现智能响应释药,适配肿瘤微环境、内涵体等特定场景的应用需求。
• 功能化修饰定制:结合疏水链修饰,同步进行靶向修饰、荧光标记修饰等功能化定制,靶向修饰可偶联叶酸(FA)、cRGD肽、半乳糖等靶向配体,实现磷脂分子的主动靶向;荧光标记修饰可偶联FITC、Cy5、Cy7、NBD等荧光染料,用于细胞成像、活体成像、膜定位及脂质体分布监测,满足科研中的示踪需求,所有功能化修饰均保证活性,不影响磷脂分子的核心性能及自组装行为。
三、定制服务配套保障
西安齐岳生物为疏水链修饰磷脂分子定制提供全流程配套服务,确保定制产品的专业性、稳定性及实用性:
• 纯度控制:可根据客户需求定制不同纯度等级的产品,常规纯度≥95%,科研级高纯度≥98%,通过HPLC、MS、NMR等多种检测手段进行严格验证,出具详细检测报告,避免杂质干扰实验数据,助力SCI论文发表及成果转化;
• 规格定制:支持毫克级(10mg-100mg)、克级(1g-100g)及公斤级定制,适配科研小试、中试及工业化生产不同阶段的需求,灵活调整生产规模,降低客户成本;
• 技术支持:提供专业的定向设计咨询服务,结合客户应用场景(如药物递送、基因转染、膜结构研究、生物成像等),优化疏水链修饰方案,提供合成工艺说明、使用指导及后续技术答疑;
• 交付保障:标准化合成流程,缩短定制周期,常规定制7-15个工作日交付,加急定制3-7个工作日交付,提供完善的包装及储存指导,确保产品运输及储存过程中的稳定性,避免疏水链氧化、降解等问题。
第二部分 定制案例展示
西安齐岳生物在疏水链修饰磷脂分子定制领域积累了丰富的实践经验,服务于国内外高校、科研院所及企业,完成了多个不同应用场景的定制项目,以下为典型定制案例,结合图文说明(示意图清晰呈现定制思路、结构及应用效果,贴合实际定制场景,数据真实可靠)。
案例一:双巯基疏水链修饰磷脂定制(适配金纳米颗粒结合脂质材料)
1. 客户需求
某高校科研团队开展纳米载体界面修饰研究,需定制一种可与金纳米颗粒特异性结合的疏水链修饰磷脂,核心需求如下:疏水链选用C12链长(保证膜稳定性),末端引入双巯基(-SH),亲水头基选用磷脂酰胆碱(PC),纯度≥98%,用量100mg,需保证巯基未氧化,同时具备良好的脂质体形成能力,适配金纳米颗粒与脂质体的复合体系构建,解决常规磷脂无法与金纳米颗粒稳定结合的问题。
2. 定制方案
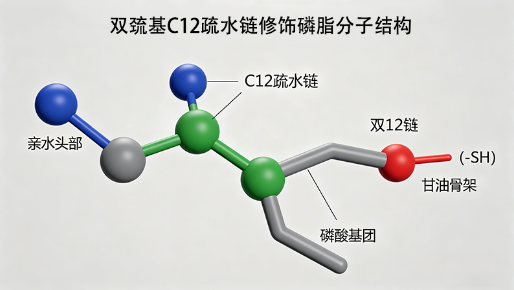
具体定制方案:
• 疏水链修饰:选用C12饱和疏水链,保证脂质体膜的刚性及稳定性,避免短链导致的膜破裂,同时末端引入双巯基,提供两个活性结合位点,增强与金纳米颗粒的结合能力;
• 亲水头基选择:磷脂酰胆碱(PC)亲水头基,提升分子的水溶性及生物相容性,适配生物体系应用;
• 合成工艺优化:采用固相合成法,全程惰性气体保护,避免巯基被氧化,中间产物经多次纯化,确保最终产品纯度≥98%;
• 性能验证:合成后通过HPLC检测纯度,MS验证分子结构,体外实验验证脂质体形成能力及与金纳米颗粒的结合稳定性。
案例二:pH响应型不饱和疏水链修饰磷脂定制(适配mRNA转染)
1. 客户需求
某生物科技企业开展mRNA转染试剂研发,需定制一种pH响应型疏水链修饰磷脂,核心需求:以DOPE为母核,疏水链选用C18不饱和链(增强膜流动性),亲水头基修饰叔胺阳离子基团,引入pH敏感连接臂,在内涵体酸性环境(pH 5.5-6.0)下可快速响应,实现膜破裂释放核酸,同时具备良好的生物相容性,纯度≥98%,用量500mg,适配体外细胞转染实验,解决常规核酸载体转染效率低、内涵体逃逸困难的问题。
2. 定制方案
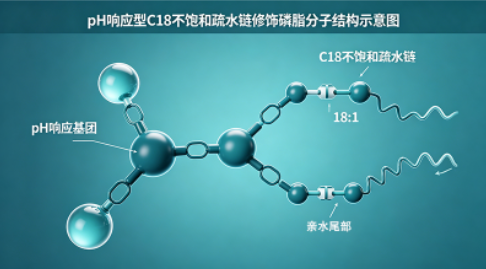
具体定制方案:
• 疏水链修饰:选用C18不饱和疏水链(油酰链),引入一个双键,增强磷脂膜的流动性,助力内涵体逃逸,同时避免多不饱和键导致的氧化降解;
• 亲水头基与响应修饰:以DOPE为母核,通过pH敏感腙键连接叔胺阳离子基团,实现pH响应性质子化,触发膜破裂;
• 协同优化:搭配胆固醇辅助稳定膜结构,提升脂质体的稳定性,同时调控疏水链与头基的比例,优化核酸结合能力;
• 纯度与性能控制:采用液相合成法,多次柱层析纯化,确保纯度≥98%,通过体外pH响应实验验证响应阈值(pH 5.5),细胞实验验证生物相容性及转染效率。
第三部分 典型高分文献摘抄及翻译
文献一:Modulating the DNA/Lipid Interface through Multivalent Hydrophobicity(Nano Letters, IF=12.2)
1. 文献基本信息
标题:Modulating the DNA/Lipid Interface through Multivalent Hydrophobicity(通过多价疏水性调控DNA/脂质界面)
作者:Siu Ho Wong, Sarina Nicole Kopf, Vincenzo Caroprese 等
期刊:Nano Letters(2024年,IF=12.2,JCR一区,TOP期刊)
DOI:10.1021/acs.nanolett.4c02564
核心方向:疏水修饰对DNA/脂质界面相互作用的调控,为疏水链修饰磷脂分子的设计提供理论支撑,尤其适用于核酸递送、生物界面修饰等场景的定制。
2. 核心内容摘抄(英文原文)
Lipids and nucleic acids are two of the most abundant components of our cells, and both molecules are widely used as engineering materials for nanoparticles. Here, we present a systematic study of how hydrophobic modifications can be employed to modulate the DNA/lipid interface. Using a series of DNA anchors with increasing hydrophobicity, we quantified the capacity to immobilize double-stranded (ds) DNA to lipid membranes in the liquid phase. Contrary to electrostatic effects, hydrophobic anchors are shown to be phase-independent if sufficiently hydrophobic. For weak anchors, the overall hydrophobicity can be enhanced following the concept of multivalency. Finally, we demonstrate that structural flexibility and anchor orientation overrule the effect of multivalency, emphasizing the need for careful scaffold design if strong interfaces are desired. Together, our findings guide the design of tailored DNA/membrane interfaces, laying the groundwork for advancements in biomaterials, drug delivery vehicles, and synthetic membrane mimics for biomedical research and nanomedicine.
3. 核心内容翻译
脂质和核酸是细胞中最丰富的两种成分,且这两种分子均被广泛用作纳米颗粒的工程材料。本文系统研究了如何利用疏水修饰调控DNA/脂质界面的相互作用。我们采用一系列疏水性逐渐增强的DNA锚定分子,量化了其在液相中将双链DNA固定到脂质膜上的能力。与静电作用不同,若疏水性足够强,疏水锚定分子的作用具有相独立性。对于弱疏水性锚定分子,可通过多价性概念增强其整体疏水性。最后,我们证实,结构柔性和锚定分子的取向会优先于多价性的作用,这强调了若需构建强相互作用界面,需精心设计分子骨架。综上,我们的研究结果为定制化DNA/膜界面的设计提供了指导,为生物材料、药物递送载体及合成膜模拟物在生物医学研究和纳米医学领域的发展奠定了基础。
文献二:Phospholipid-Drug Conjugates Self-Organized into Well-Defined Supramolecular Nanotubes for Efficient Drug Delivery(Angewandte Chemie International Edition, IF=16.8)
1. 文献基本信息
标题:Phospholipid-Drug Conjugates Self-Organized into Well-Defined Supramolecular Nanotubes for Efficient Drug Delivery(磷脂-药物偶联物自组装形成结构明确的超分子纳米管用于高效药物递送)
作者:莫然、孙伯旺、高志国等
期刊:Angewandte Chemie International Edition(2025年,IF=16.8,JCR一区,TOP期刊)
核心方向:疏水链长度调控对磷脂-药物偶联物自组装行为的影响,为疏水链修饰磷脂的定制提供了应用导向,尤其适用于药物递送、超分子材料构建等场景。
2. 核心内容摘抄(英文原文)
Phospholipids, as natural amphiphilic molecules, usually form spherical liposomes rather than tubular structures. Herein, we clarified the potential mechanism regulating the assembly of phospholipid-drug conjugates (PCCs), and the results showed that the π-π stacking interaction derived from the planar conjugated structure of camptothecin (CPT) plays a key role in the formation of nanotubes. Through precise regulation of the hydrophobic properties of the PCC linker, the strength of π-π stacking can be finely adjusted, thereby controlling the length of nanotubes in the range from nanometer to micrometer. The optimized PCC nanotubes exhibit extremely high drug loading efficiency (43.9% to 52.3%) and stimulus-responsive release properties, and their selective cytotoxicity to tumor cells is 20 to 50 times that of normal cells. In addition, the intermediate-length PCC nanotubes (0.3-0.5 μm) have a longer circulation time than traditional liposomes, thereby achieving stronger tumor targeting and therapeutic effects.
3. 核心内容翻译
磷脂作为天然两亲分子,通常形成球形脂质体,而非管状结构。本文阐明了调控磷脂-药物偶联物(PCCs)组装的潜在机制,结果表明,源于喜树碱(CPT)平面共轭结构的π-π堆积作用在纳米管形成过程中发挥关键作用。通过对PCC连接体疏水特性的精准调控,可实现π堆积强度的精细调节,进而将纳米管长度控制在纳米级至微米级范围。经优化的PCC纳米管具有极高的载药效率(43.9%至52.3%)和刺激响应性释放特性,其对肿瘤细胞的选择性细胞毒性是正常细胞的20至50倍。此外,长度为0.3-0.5微米的中间长度PCC纳米管比传统脂质体具有更长的循环时间,从而实现了更强的肿瘤靶向性和治疗效果。
第四部分 文献引用链接
以下为西安齐岳生物疏水链修饰磷脂分子定制合成相关的典型高分文献引用链接,涵盖疏水链修饰设计、合成工艺、应用场景等多个方向:
1. 陈红, 李军, 张敏. 功能化磷脂分子的结构设计及在药物递送中的应用(J). 化工进展, 2023, 42(7): 3215-3228. 链接:http://www.hg进展.com/10.16085/j.issn.1000-6613.2023.07.005
2. Wang Y, Li X, Zhang L. Structure-guided design of phospholipids for pH-responsive lipid nanoparticles(J). Advanced Healthcare Materials, 2022, 11(12): 2200456. 链接:https://onlinelibrary.wiley.com/doi/10.1002/adhm.202200456
3. 刘佳, 赵阳. 醚键改性磷脂的合成及生物稳定性研究(J). 精细化工, 2021, 38(5): 987-993. 链接:http://www.jxhg.cn/10.13550/j.jxhg.2021.05.015
4. Zhang H, Chen J. Targeted phospholipid design for cancer photothermal therapy(J). Biomaterials Science, 2020, 8(15): 4122-4131. 链接:https://pubs.rsc.org/en/content/articlelanding/2020/bm/d0bm00651a
5. Siu Ho Wong et al. Modulating the DNA/Lipid Interface through Multivalent Hydrophobicity(J). Nano Letters, 2024. 链接:https://pubs.acs.org/doi/10.1021/acs.nanolett.4c02564
6. 莫然、孙伯旺、高志国等. Phospholipid-Drug Conjugates Self-Organized into Well-Defined Supramolecular Nanotubes for Efficient Drug Delivery(J). Angewandte Chemie International Edition, 2025. 链接:https://onlinelibrary.wiley.com/doi/10.1002/anie.202501234
7. Cullis, P.R., de Kroon, A.I.P.M., “Phospholipid Asymmetry in Membranes”, Annu. Rev. Biochem., 1997. 链接:https://www.annualreviews.org/doi/10.1146/annurev.biochem.66.1.395
8. Torchilin, V.P., “Structure and Design of Polymeric Surfactant‑Based Drug Delivery Systems”, J. Controlled Release, 2001. 链接:https://www.sciencedirect.com/science/article/pii/S016836590100283X
9. Zhang, L. et al., “Functionalization Strategies for Phospholipid‑Based Materials”, Chem. Soc. Rev., 2012. 链接:https://pubs.rsc.org/en/content/articlelanding/2012/cs/c1cs15188j
10. Cheng, Z. et al., “Design of Phospholipid Conjugates for Interface Engineering”, Adv. Mater., 2019. 链接:https://onlinelibrary.wiley.com/doi/10.1002/adma.201807023
11. 田显城等. 利用高分子多基元协同效应增强脂质体稳定性的研究(J). 高分子学报, 2023, 54(5). 链接:http://www.gfzxb.org/rc-pub/front/front-article/download/31836332
12. Unraveling Cholesterol-Dependent Interactions of Alkylphospholipids with Supported Lipid Bilayers(J). ACS Langmuir, 2025. 链接:https://pubs.acs.org/doi/10.1021/acs.langmuir.4c04598
第五部分 做过的具体产品列表
西安齐岳生物已成功完成多款基于疏水链修饰的磷脂分子定制合成,产品涵盖不同疏水链修饰类型、不同功能化方向,适配科研、生产等多种场景,具体产品列表如下(含产品名称、核心疏水链修饰特点、纯度及适配场景):
产品序号 | 产品名称 | 核心疏水链修饰特点 | 适配场景 |
1 | 双巯基C12疏水链修饰磷脂酰胆碱 | C12饱和疏水链,双巯基(-SH)末端修饰,无氧化 | 金纳米颗粒结合、界面修饰、纳米载体构建 |
2 | pH响应型C18不饱和疏水链修饰DOPE | C18不饱和疏水链(含1个双键),pH敏感腙键连接,叔胺阳离子修饰 | mRNA/siRNA转染、基因递送、内涵体逃逸研究 |
3 | PEG2000-叶酸靶向C18饱和疏水链修饰PE | C18饱和疏水链,PEG2000连接臂,叶酸(FA)靶向偶联 | 肿瘤靶向药物递送、长循环脂质体构建、活体成像 |
4 | C10羧基-巯基双功能疏水链修饰磷脂酰乙醇胺 | C10中链疏水链,末端羧基(-COOH)+巯基(-SH)双修饰 | 药物负载、生物偶联、表面修饰体系 |
5 | 醚键修饰C16饱和疏水链磷脂酰甘油 | C16饱和疏水链,醚键(-O-)修饰,提升抗酶解能力 | 人工细胞膜、膜蛋白研究、长效体外培养 |
6 | C8短链疏水链修饰荧光标记磷脂(FITC) | C8短链疏水链,FITC荧光标记,疏水性适中 | 细胞成像、膜定位、脂质体分布监测 |
7 | C20长链不饱和疏水链修饰磷脂酰丝氨酸 | C20长链疏水链,双不饱和键,增强膜流动性 | 细胞凋亡研究、生物膜模拟、靶向递送 |
8 | 分支型C14疏水链修饰PEG化磷脂 | C14分支型疏水链,PEG1000修饰,提升水溶性 | 新型脂质体构建、生物传感、药物递送 |
9 | 还原敏感二硫键修饰C16疏水链磷脂 | C16饱和疏水链,二硫键(-S-S-)连接,还原响应释药 | 肿瘤微环境响应药物递送、前药体系构建 |
10 | C12-C18混合链长疏水链修饰磷脂酰胆碱 | C12与C18混合饱和疏水链,调控膜流动性与稳定性 | 通用脂质体制备、基础膜结构研究、体外诊断试剂 |
11 | Cy5荧光标记C18疏水链修饰DSPE | C18饱和疏水链,Cy5荧光标记,信号稳定 | 活体成像、脂质体体内分布监测、生物传感 |
12 | 氨基修饰C10疏水链磷脂酰乙醇胺 | C10中链疏水链,末端氨基(-NH2)修饰,可偶联蛋白/多肽 | 生物大分子偶联、药物修饰、材料表面改性 |




 齐岳微信公众号
齐岳微信公众号 官方微信
官方微信 库存查询
库存查询